Praktikum am Dlfe
im Herbst 2019
Von Antje Soeken
Dank der Auricher Wissenschaftstage wurde es mir ermöglicht, in den Herbstferien ein zweiwöchiges Praktikum, am Deutschen Institut für Ernährungsforschung in Potsdam zu machen. Ich wollte ein Praktikum am Deutschen Institut für Ernährungsforschung machen, da ich mich beruflich im Bereich der Ernährung orientieren möchte. Am Deutschen Institut für Ernährungsforschung war ich dem Bereich der Diabetologie, unter der Leitung der Professorin Schürmann zugeteilt. Mein Ansprechpartner war Dr. Leager, der Postdoc von meiner Betreuerin Teresa.
Tag 1
Am ersten Tag wurde ich von der Sekretärin empfangen, welche mir das Institut zeigte und einen Laborkittel sowie Schlüssel für Spind und Labor gab.
Anschließend wurde mir die Forschung von Dr. Leager und seinem Team vorgestellt. Die Forschung handelt von der Vermeidung der Krankheit Diabetes Typ 2. Diabetes Typ 2 ist, wenn die Organe resistent gegen Insulin, welches die Organe dazu anregen soll, Glucose aufzunehmen, werden. Falls die Organe jedoch resistent gegen Insulin sind, wird die Glucose wenig bis gar nicht aufgenommen. Das sorgt dafür, dass die Bauchspeicheldrüse mehr Insulin produziert, da sie denkt, dass noch mehr Glucose da ist, weil sie nicht aufgenommen wird. Nach einiger Zeit nimmt die Bauchspeicheldrüse dadurch großen Schaden und produziert weniger bis kein Insulin mehr. Durch die Forschung mit Diäten haben sie herausgefunden, dass der Blutzucker von Diabetikern des Typs 2 durch eine proteinarme Diät nicht so hoch ist, wie bei anderen Ernährungsformen. Dadurch stellte sich die Frage „warum?“. Warum nehmen diejenigen, die eine proteinarme Diät verfolgen, die Glucose aus dem Blut auf und diejenigen mit einer anderen Ernährung nicht? Es stellte sich heraus, dass durch eine proteinarme Diät in der Leber das Protein FGF21 hergestellt wird, welches dem Köper bemerkbar macht, dass es Energie braucht und somit die Organe anregt Glucose aufzunehmen. FGF21, was für „Fibroblast Growth Factor 21“steht, übernimmt somit die Rolle des Insulins ein. Völlig auf Proteine zu verzichten, ist jedoch sehr schwer und schon fast eine unerträgliche Diät. Daraufhin wurde überlegt, ob man nicht nur eine bestimmte Sorte von einem essenzielen Protein nimmt und zwar Methionin. Man vermeidet Methionin, indem man eine fleischarme Diät verfolgt.
Beim Teammeeting wurde ich anschließend von der Professorin begrüßt und es wurde über Aufgaben der kommenden Woche gesprochen.
Danach habe ich meiner Betreuerin Teresa dabei zugeschaut, wie sie an einem Western Plot, anhand dessen man die Größe von Proteinen bestimmen kann, gearbeitet hat.
Später habe ich Petrischalen für kommende Inselzellenforschungen präpariert.
Tag 2
Der zweite Tag begann mit dem erneuten Präparieren von Petrischalen. Danach wurde mir das Zelllabor gezeigt, in dem Zellen für verschiedene Versuche gezüchtet werden. Später habe ich mit Teresa einen Testlauf für ein Experiment für den nächsten Tag durchgeführt, indem einer Maus die Leber entnommen wird, um an Material für weitere Forschungen zu gelangen.
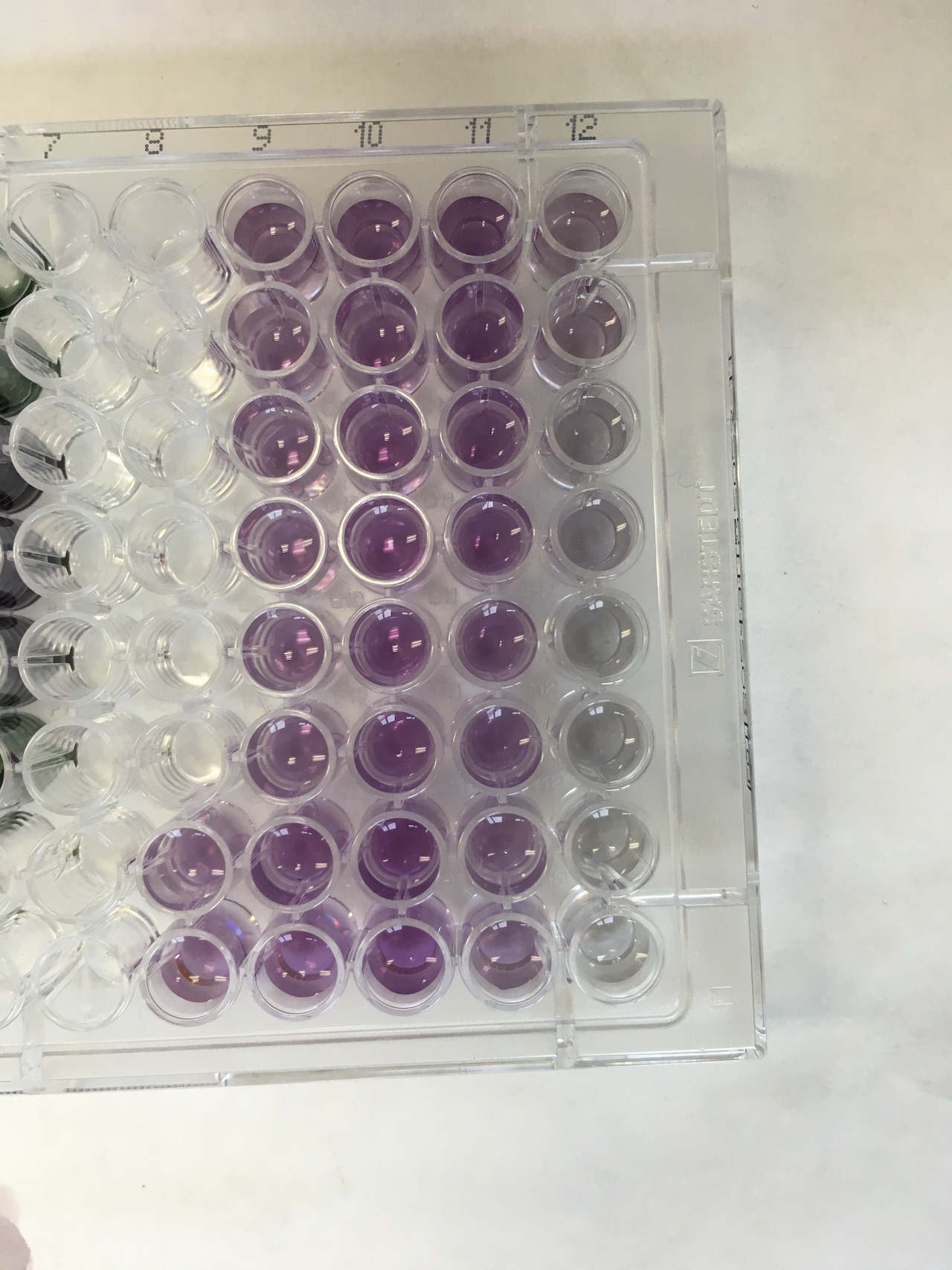
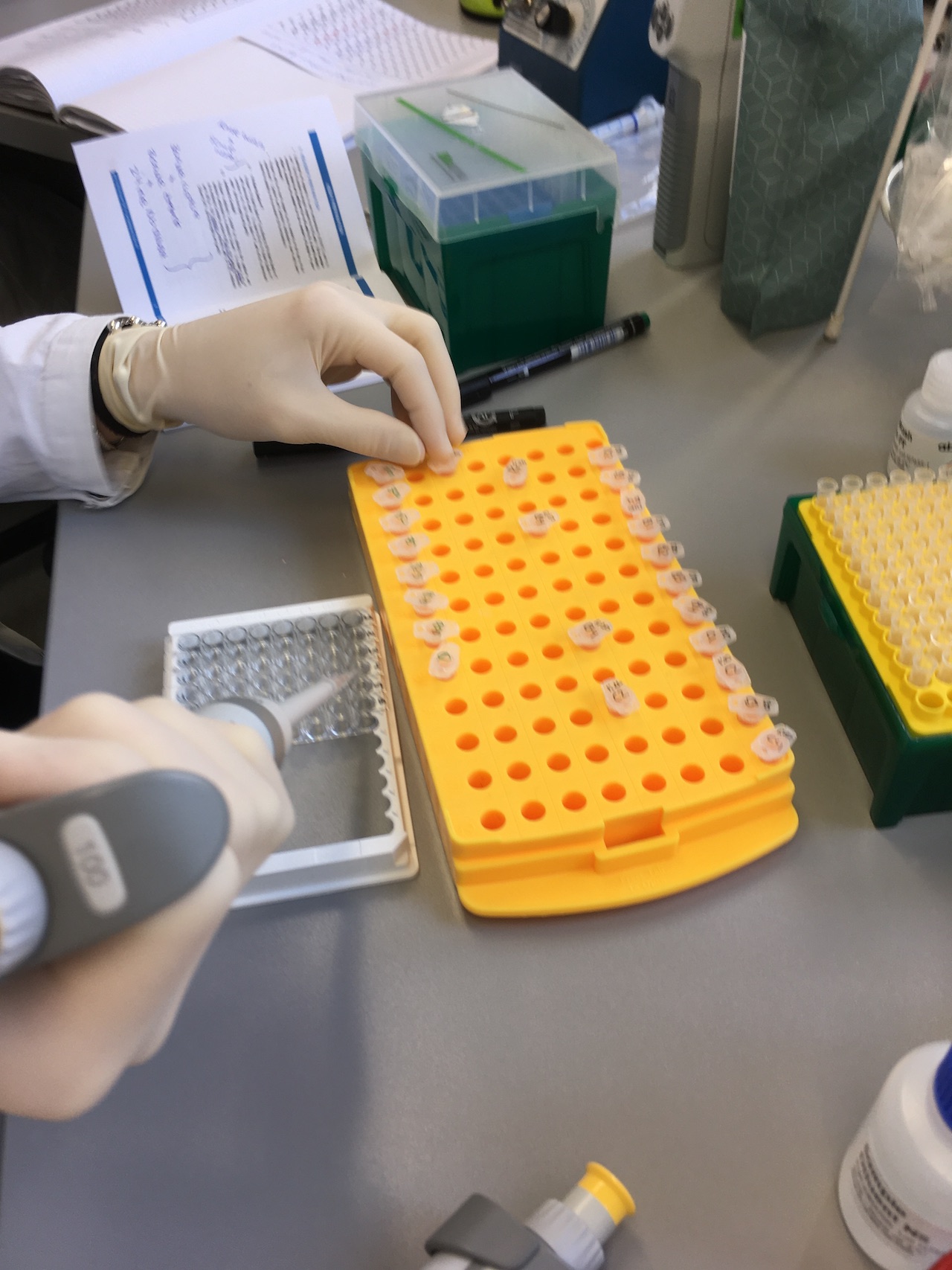
Nach der Mittagspause habe ich mit einem anderen Praktikanten eine Proteinbestimmung, in der man Proteine mit Standards vergleicht, durchgeführt. Das hat bis zum Feierabend gedauert, da wir viel pipettieren mussten, was sich als sehr zeitaufwändig erwies.
Tag 3
Am Morgen habe ich mit meiner Betreuerin das Labor, für das vorgesehene Experiment an der Maus, vorbereitet. Es handelt sich um eine B7 Maus, diese sind sehr dünn um beim Experiment circa 10- 18 Wochen alt. Wir haben alle benötigten Sachen herausgelegt und die Lösungen fürs Experiment gemischt. Nachdem alles vorbereitet war, wurde die erste Maus narkotisiert. Nach einigen Minuten wurde getestet, ob die Maus nichts mehr spürt. Danach wurde sie am Bauch geöffnet und der Margen mit dem Dünn- und Dickdarm vorsichtig aus dem Köper herausgelegt, um die Vena Cava freizulegen. In die Vena Cava wurde eine Nadel eingeführt, die den Buffer 1 durch diese pumpt. Währenddessen wird die Pfortader geöffnet, damit das Blut aus dem Köper entweichen kann. Durch den Buffer 1 wird die Leber heller und etwas größer. Nach einer Weile wird der Buffer 1 durch den Buffer 2 ausgetauscht. Der Buffer 2 sorgt dafür, dass die Leberzellen sich in der Leber lösen. Wenn die Leber schwammig wird, wird sie aus dem Köper rausgeschnitten. Die Leber wird auf einen Textilausschnitt gelegt und mit in einer Pinzette verkleinert. Die Leber wird flüssig. Danach wurden die Leberzellen in Verbindung mit Buffer 3 gebracht und zentrifugiert. Dadurch lagern sich die gewünschten Zellen am Boden ab und der „Abfall“ schwimmt im Buffer 3. Der Buffer 3 wird vorsichtig entsorgt, es wird frischer Buffer 3 zu den Leberzellen hinzugefügt und durch eine Pipette werden die Zellen vorsichtig vom Boden gelöst. Es wird nochmal zentrifugiert und noch einmal der Buffer 3 entsorgt. Danach wird ein kleiner Teil der Proteine gezählt, dass dann auf die Maße ausgerechnet und dann ausgerechnet, wie viel Mikro Liter in eine Fläche kommen. Zu den Zellen wird noch eine Substanz hinzugefügt, die wie Nahrung für die Zellen ist. Die Zellen können so ca. drei Tage überleben.
Tag 6
Am Morgen habe ich die Pipettenspitzen für den Autoklaven vorbereitet und danach die Petrischalen präpariert. Danach haben wir an das Experiment vom 09. Oktober angeknüpft. Wir haben die gewonnenen Zellen mit Antiköpern behandelt, um die Proteine von ihnen zu lösen. Diese Proteine haben wir mithilfe einer Maschine gezählt, also eine Protein Determination gemacht. Außerdem wird FGF21 gezählt, um die Abhängigkeit, beziehungsweise den Zusammenhang zwischen FGF21 und Proteine herauszufinden.
Tag 7
Am Morgen habe ich erneut Pipettenspitzen für den Autoklaven vorbeireitet. Danach wollten meine Betreuerin und ich das Experiment vom 09. Oktober wiederholen. Leider konnten wir das Experiment jedoch nicht vollenden, da es aufgrund von Problematiken, die aufgekommen sind, nicht funktioniert hat. Am Nachmittag habe ich dann einer anderen Doktorandin bei ihrer Vorarbeit für ein Experiment geholfen. Sie hat acht Mäusen die
Organe entnommen, welche ich dann gewogen und dokumentiert habe. Außerdem habe ich den Blutzuckerspiegel der Mäuse gemessen. Danach habe ich die Organe mithilfe von flüssigem Stickstoff eingefroren.

Tag 8
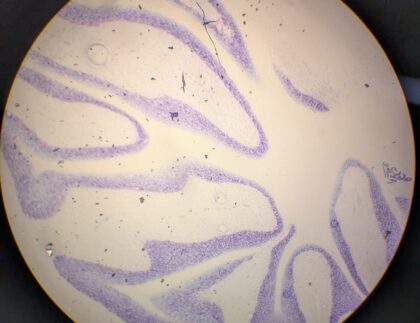
Am achten Tag habe ich zunächst dabei zugeschaut, wie wir Mäuse, um an die Pankreas zu kommen, getötet haben. Als die Pankreas freigelegt war, wurde Collagenase in das anliegende Blutgefäß gespritzt, wodurch die Pankreas angeschwollen ist und zu einer gelartigen Masse wurde. Anschließend wurde die Pankreas mit so wenig Kontakt wie möglich aus dem Körper der Maus geborgen, damit keine Inselzellen austreten. Den Vorgang haben wir an sieben weiteren Mäusen wiederholt. Dann hat meine Betreuerin, die Inselzellen innerhalb der einzelnen Pankreas gezählt. Am Nachmittag habe ich, um das Pipettieren zu üben, mit der labortechnischen Assistentin erneut eine Proteinbestimmung durchgeführt, da das Pipettieren eine wichtige Fertigkeit im Bereich der Forschung im Labor ist.
Tag 9
An diesem Tag haben wir einen Western Blot gemacht. Dabei werden Proteine auf ein Trägermembran übertragen. Dazu haben wir zunächst ein Gel hergestellt, welches einige Zeit ruhen musste. Anschließend haben wir sehr kleine Farbpigmente hinzugefügt. Dann wurde das Gel in ein Gerät getan, welches mit Flüssigkeit gefüllt und unter Strom gesetzt worden war, sodass die Proteine durch das Gel hindurch nach unten fließen. Nach ca. eineinhalb Stunden sind die Farbpigmente nach ganz unten gelangt und im Gel sind vereinzelt kleine Farbmarkierungen aufgetreten. Danach wird das Gel auf ein Membranpapier gelegt und ummantelt von Filterpapier und Schwämmen sowie in ein weiteres Gerät gelegt, das dafür sorgt, dass sich die Proteine aus dem Gel auf das Membranpapier übertragen. Später wird das Membranpapier einige Male mit einer Lösung gewaschen und dann mit einer milchartigen Substanz potenziert. Nach ca. 30 Minuten wird es in einer kalten Umgebung weiter potenziert.
Tag 10
Am letzten Tag habe ich bestimmte Substanzen für weitere Experimente präpariert. Außerdem habe ich das Membranpapier mehrmals gewaschen und getrocknet. Anschließend haben wir es in einer Maschine ausgewertet. Zur Mittagszeit habe ich mich auf meine Abreise begeben.
Fazit
Das Praktikum am DIfE hat mir sehr gut gefallen, da ich sehr herzlich aufgenommen wurde und es sehr lehrreich für mich war. Es hat viel Spaß gemacht und war sehr interessant zu sehen, wie es in einem Labor abläuft. Besonders gut hat mir die Laborarbeit gefallen.
Ich hatte zudem eine Einsicht in die Forschung bekommen und kann mir jetzt erst richtig vorstellen, wie diese abläuft. Es hat viel mit Büroarbeit zutun und man muss viel recherchieren und beantragen bevor man überhaupt loslegen kann. Mir wurde auch klar, dass viele Forschungen nicht funktionieren und es eine echte Geduldssache ist, um in der Forschung voran zu kommen. Es war ein schöner Einblick in die Berufswelt. Ich habe viele Leute kennengelernt, die alle in unterschiedlichen Bereichen studiert haben und habe viele Tipps bekommen.